Mirai significa futuro in giapponese e sora è cielo. Un glossario delle parole chiave per orientarsi durante le Olimpiadi di Tokyo 2020 e scoprire il piano di mobilità sostenibile dei giochi, realizzato insieme a un partner d’eccezione.
La ricerca nel settore dei veicoli a basso impatto ambientale ha portato a considerare l’utilizzo dell’idrogeno nelle fuel cells. Ecco come fuonziano
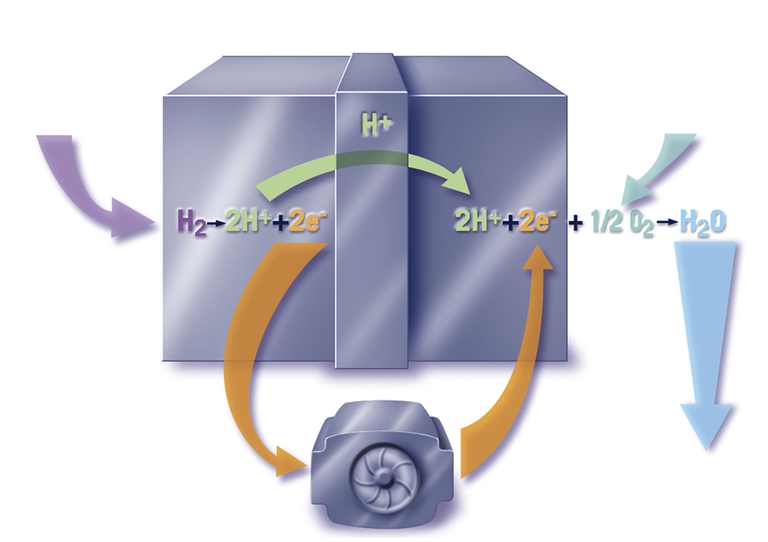
Le fuel cell funzionano grazie alla trasformazione dell’energia chimica contenuta in un combustibile direttamente in energia elettrica, arrivando così ad ottenere un rendimento “termochimico” idealmete unitario. L’energia così prodotta può essere facilmente stivata all’interno di accumulatori o direttamente sfruttata da un motore elettrico.
Il tutto funziona senza alcuna fiamma libera ma all’interno della fuel cell stessa. Questa applicazione ha senza dubbio enormi vantaggi e applicazioni. Al momento appare assai interessante la possibilità di utilizzare celle (o pile) ad idrogeno già impiegate per applicazioni spaziali dalle missioni Apollo.
Sull’elettrodo positivo (anodo) della cella, saturo dell’ossigeno presente nell’aria, avviene la riduzione dell’ossigeno stesso mentre sul catodo avviene l’ossidazione dell’idrogeno. Come risultato della reazione, oltre all’energia elettrica e a una certa quantità di calore generati, si ha la produzione di acqua; i due elettrodi sono immersi nell’elettrolita, una soluzione concentrata di idrossido di potassio (KOH), e rivestiti da catalizzatori per aumentare la velocità delle reazioni elettrodiche.
Il problema di utilizzare direttamente l’idrogeno risiede sia nello stivaggio a bordo del veicolo che nella possibilità di creare delle idonee strutture di distribuzione. Infatti l’idrogeno è altamente infiammabile e va conservato a temperature assai basse. Comunque, per la soluzione del problema dello stivaggio a bordo, sono allo studio particolari serbatoi che potrebbero rispondere a tutti i requisiti di sicurezza; essi, realizzati in forma cilindrica contengono una intercapedine ove è creato il vuoto pneumatico, consentono la conservazione dell’idrogeno liquido a temperature prossime ai -250 °C.
Una soluzione intermedia è rappresentata dall’applicazione di un reformer per ottenere l’idrogeno da un combustile più stabile e più sicuro quali sono i gas naturali ed i prodotti petroliferi. Particolare attenzione è rivolta alla possibilità di utilizzare il metanolo (CH3OH) che il reformer, attraverso la sezione a bruciatore, vaporizza insieme all’acqua e, con una successiva sezione, ossida l’ossido di carbonio (CO) convertendolo in CO2.
La reazione è così sintetizzabile:
CH3OH+H2O -> 3H2+CO
Si noti che l’acqua necessaria al funzionamento del reformer può essere ricavata direttamente come prodotto della reazione nella pila rendendo continuo e autosufficiente il ciclo di conversione. La catena energetica dei veicoli a cella a combustibile necessita, come per i normali veicoli a batteria, della conversione dell’energia attraverso dispositivi elettronici di potenza e comunque di un certo numero di batterie per costituire un valido volano energetico per rispondere adeguatamente ai picchi di assorbimento di corrente.
La necessità dell’uso del reformer non eliminerebbe completamente dipendenza dai derivati petrolio, ma consentirebbe comunque di ottenere rendimenti energetici del carburante prossimi al 70% e di abbattere drasticamente le immissioni nell’atmosfera.
Siamo anche su WhatsApp. Segui il canale ufficiale LifeGate per restare aggiornata, aggiornato sulle ultime notizie e sulle nostre attività.
![]()
Quest'opera è distribuita con Licenza Creative Commons Attribuzione - Non commerciale - Non opere derivate 4.0 Internazionale.
Mirai significa futuro in giapponese e sora è cielo. Un glossario delle parole chiave per orientarsi durante le Olimpiadi di Tokyo 2020 e scoprire il piano di mobilità sostenibile dei giochi, realizzato insieme a un partner d’eccezione.
A San Francisco sono al lavoro per terminarlo entro il 2019. Servirà i turisti della baia della città, senza inquinare come le altre imbarcazioni.
Lo hamesso a punto un gruppo di ricercatori in Svizzera. Esposto alla luce, separa le molecole di acqua in ossigeno e idrogeno e degrada le sostanze inquinanti.
Il motore del futuro potrà essere alimentato a gas naturale, idrogeno o batterie. Sarà intelligente e capace di adattarsi a impieghi diversi. Lo ha spiegato al Tech Day 2018 di Torino Annalisa Stupenengo, presidente di FPT Industrial.
L’idrogeno ha le carte in regola per essere la tecnologia del futuro: lo hanno dimostrato l’Energy Observer e la Toyota Mirai, protagonisti di un evento nella città lagunare.
Non poteva che essere il figlio di un autista di autobus, oggi divenuto sindaco di Londra, ad inaugurare il primo bus a idrogeno della capitale inglese. È stato infatti Sadiq Khan a portare il famoso double-decker rosso a zero emissioni, sulle strade londinesi. A produrlo la nord irlandese Wrightbus, specializzata proprio nella realizzazione di autobus
L’idrogeno vive e combatte con noi. Sebbene l’attenzione mediatica del momento sia attratta principalmente dalla propulsione ibrida, ibrida plug-in ed elettrica (a batteria), la mobilità a idrogeno è tutt’altro che accantonata. Alla realizzazione delle prime vetture di serie, vale a dire la SUV Hyundai ix35 Fuel Cell e le berline Toyota Mirai e Honda Clarity
Si trova in Auchtertstraße 19 in Metzingen, la 22ma stazione di rifornimento a idrogeno della Germania. Fa parte del corridoio Stoccarda-Monaco ed è stata inaugurata lo scorso 26 settembre. Si allunga così la lista delle stazioni già operative nel Paese e rende più vicino l’obiettivo di una rete nazionale di rifornimento. “Mobilità pulita,
Risultati entusiasmanti nella gara per auto a bassi consumi. Gli studenti italiani vincono le categorie a idrogeno e batterie.