Un rapporto del think tank Ember evidenzia l’autentico boom delle energie rinnovabili nei 74 paesi del Climate vulnerable forum.
Le fuel cell consentono di produrre energia elettrica. Funzionamento e i campi d’utilizzo: ecco motivata la scelta dell’idrogeno come combustibile.
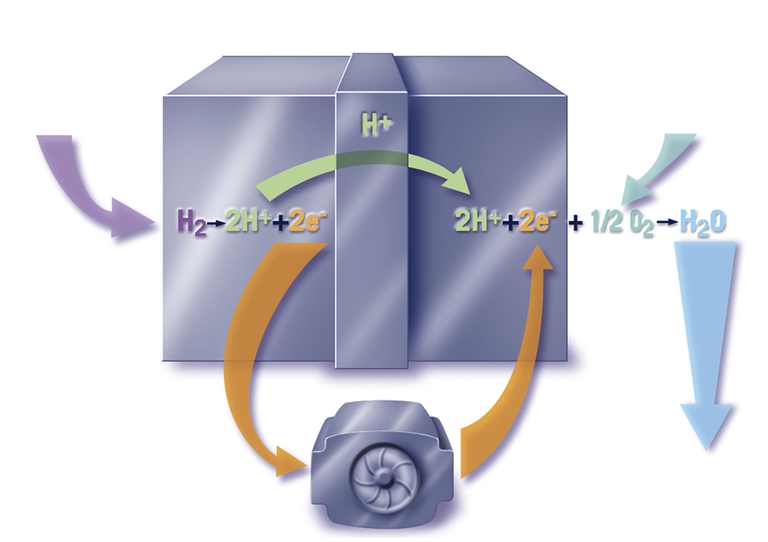
Una fuel cell è un dispositivo che converte l’energia chimica di un combustibile in energia elettrica e calore senza utilizzare cicli termici.
Le celle a combustibile alimentate a idrogeno (H2) consentono di produrre energia elettrica e acqua calda a partire da idrogeno e ossigeno.
Il processo che avviene al loro interno è esattamente contrario all’elettrolisi: quando si scinde l’acqua (H2O) in H2 ed O2 è necessario fornire corrente, invertendo il processo si produce corrente e acqua.
L’idrogeno è un gas in grado di essere ionizzato facilmente, perché la sua molecola è costituita da due atomi legati da un legame relativamente debole. ll comburente più usato è l’ossigeno, abbondante, disponibile gratuitamente in atmosfera e in grado di reagire con l’idrogeno dando un prodotto innocuo come l’acqua.
Sull’elettrodo positivo (anodo) della cella, saturo dell’ossigeno presente nell’aria, avviene la riduzione dell’ossigeno stesso mentre sul catodo avviene l’ossidazione dell’idrogeno. Come risultato della reazione, oltre all’energia elettrica e a una certa quantità di calore generati, si ha la produzione di acqua; i due elettrodi sono immersi nell’elettrolita, una soluzione concentrata di idrossido di potassio (KOH), e rivestiti da catalizzatori per aumentare la velocità delle reazioni elettrodiche.
Attualmente esistono sei tipologie di celle a combustibile impiegate nella produzione di energia elettrica centralizzata o distribuita, generazione di calore o per il trasporto.
Le celle a combustibile, grazie alle loro caratteristiche, presentano molteplici vantaggi sia dal punto di vista energetico sia da quello ambientale. Possiedono infatti:
Il problema di utilizzare direttamente l’idrogeno nelle fuel cell impiegate per i sistemi di trazione risiede sia nello stivaggio a bordo del veicolo sia nella possibilità di creare delle idonee strutture di distribuzione. Infatti l’idrogeno è altamente infiammabile e va conservato a temperature molto basse. Per la soluzione del problema dello stivaggio a bordo, sono allo studio particolari serbatoi che potrebbero rispondere a tutti i requisiti di sicurezza; realizzati in forma cilindrica i serbatoi presentano un’intercapedine dove viene creato il vuoto pneumatico, consentendo così la conservazione dell’idrogeno liquido a temperature prossime ai -250 °C.
Oggi, una soluzione intermedia è rappresentata dall’applicazione di un reformer per ottenere l’idrogeno da un combustile più stabile e più sicuro quali sono i gas naturali e i prodotti petroliferi. Particolare attenzione è rivolta alla possibilità di utilizzare il metanolo (CH3OH) che il reformer, attraverso la sezione a bruciatore, vaporizza insieme all’acqua e, con una successiva sezione, ossida l’ossido di carbonio (CO) convertendolo in CO2.
La reazione è così sintetizzabile:
CH3OH+H2O -> 3H2+CO
L’acqua necessaria al funzionamento del reformer può essere ricavata direttamente come prodotto della reazione nella pila rendendo continuo e autosufficiente il ciclo di conversione. La catena energetica dei veicoli a cella a combustibile necessita, come per i normali veicoli a batteria, della conversione dell’energia attraverso dispositivi elettronici di potenza e comunque di un certo numero di batterie per costituire un valido volano energetico per rispondere adeguatamente ai picchi di assorbimento di corrente.
La necessità dell’uso del reformer non eliminerebbe completamente la dipendenza dai derivati petrolio, ma consentirebbe comunque di ottenere rendimenti energetici del carburante prossimi al 70% e di abbattere drasticamente le immissioni nell’atmosfera.
Siamo anche su WhatsApp. Segui il canale ufficiale LifeGate per restare aggiornata, aggiornato sulle ultime notizie e sulle nostre attività.
![]()
Quest'opera è distribuita con Licenza Creative Commons Attribuzione - Non commerciale - Non opere derivate 4.0 Internazionale.
Un rapporto del think tank Ember evidenzia l’autentico boom delle energie rinnovabili nei 74 paesi del Climate vulnerable forum.
Con il decreto Bollette slitta la dismissione definitiva, che doveva arrivare già a fine 2025: ecco come si è arrivati alla situazione di oggi.
Ufficiale l’impegno al rafforzamento, nel mix energetico, della quota prodotta con i reattori di terza e quarta generazione. Ecco come ci siamo arrivati.
Nel 2025 l’Italia, anche grazie a Erion Energy, ha raccolto 6.200 tonnellate di batterie esauste, ma siamo lontani dai target europei.
Un rapporto di Ember spiega che nel 2025 la produzione di energia elettrica da solare, eolico e idroelettrico ha superato quella da fonti fossili.
Il modello virtuoso e sostenibile delle comunità energetiche rinnovabili sta riscontrando un successo innegabile in Italia.
Le rinnovabili hanno prodotto più energia elettrica del carbone, ma l’obiettivo di triplicarne la capacità installata appare ormai fuori portata.
Come funziona la geotermia e perché soddisfa solo lo 0,3 per cento dell’elettricità mondiale. Storia di una fonte energetica trascurata.
Mezzi danneggiati, operai minacciati: in Toscana è scontro sull’opera. Marco Duranti, presidente di Legambiente Firenze, spiega che il parco è necessario.